
Содержание
- направления
- Количество электронов в валентном слое
- Структура Льюиса
- Формальный заряд каждого атома
- предупреждение
- Что вам нужно
При определении формального заряда молекулы, такой как CoCl2 (газ фосген), необходимо знать количество электронов в валентном слое каждого атома и структуру Льюиса молекулы.
направления
-
Ищите каждый атом в периодической таблице элементов, чтобы определить количество электронов в валентном слое.
-
Напомним, что два электрона находятся на первом подуровне s, два находятся на втором подуровне s, шесть электронов на первом подуровне p и так далее. Вспомните: 1s (^ 2) 2s (^ 2) 2p (^ 6) 3s (^ 2) 3p (^ 6).
-
Хит груз. Если молекула представляет собой ион, добавьте или вычтите один или несколько электронов из общего количества, чтобы достичь окончательного заряда.
-
Для CoCl2 (газообразный фосген): C = 4; О = 6; Cl = 7. Молекула не ионизирована и имеет нейтральный заряд. Поэтому общее число электронов в валентном слое составляет 4 + 6 + (7x2) = 24.
Количество электронов в валентном слое
-
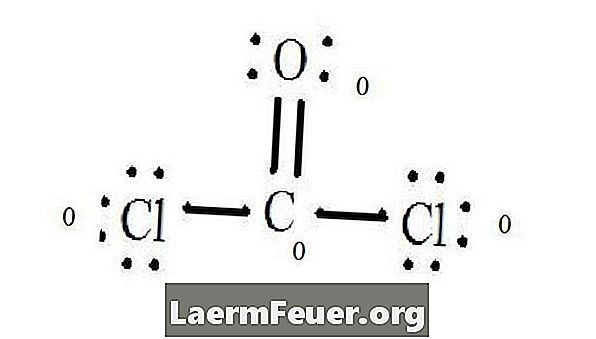
См. Структурную диаграмму Льюиса CoCl2 (газообразный фосген). Структура Льюиса представляет собой наиболее стабильную и вероятную структуру молекулы. Атомы нарисованы с парными валентными электронами; связи образуются между свободными электронами для удовлетворения правила октета.
-
Нарисуйте каждый атом и его валентные электроны, а затем сформируйте связи по мере необходимости.
Электроны, нарисованные на структуре Льюиса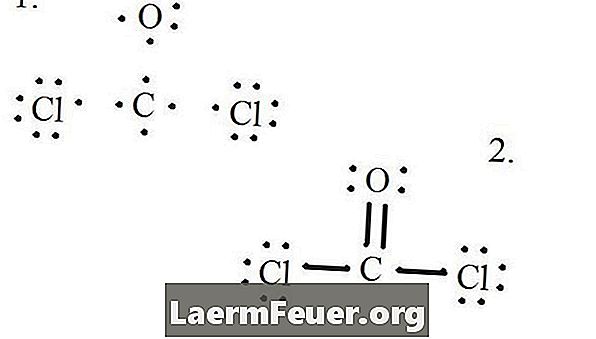
-
Атомы хлора имеют одинарные связи с молекулой углерода, а атом кислорода образует двойную связь с углеродом. Каждый атом в конечной структуре удовлетворяет правилу октета и имеет восемь электронов в валентном слое, что обеспечивает молекулярную стабильность.
Структура Льюиса
-
Подсчитайте пары свободных электронов каждого атома в структуре Льюиса. Каждый атом обозначает электрон каждой связи, в которой он участвует. Добавьте эти числа. В CoCl2: C = 0 свободных пар плюс 4 связывающих электрона = 4 электрона. O = 4 электрона свободных пар плюс 2 электрона связей = 6 электронов. Cl = 6 электронов свободных пар плюс один электрон одной связи с C = 7 электронами.
-
Вычтите количество электронов в валентном слое на несвязанном атоме. Результатом является формальный заряд для каждого атома. В CoCl2: C = 4 валентных электрона (ev) в несвязанном атоме минус 4 электрона, обозначенных в структуре Льюиса (LS) = 0 формального заряда O = 6 ev - 6 LS = 0 формального заряда Cl = 7 и - 7 LS = 0 официальных сборов
Формальные заряды атомов
-
При записи поместите эти заряды рядом с атомами в структуре Льюиса. Если в сумме у молекулы есть заряд, поместите структуру Льюиса в скобки с записью заряда в правом верхнем углу.
Формальный заряд каждого атома
предупреждение
- Расчет формального заряда для молекул, содержащих переходные металлы, может быть коварным. Количество электронов в валентном слое для переходных металлов будет таким, которое находится вне структуры благородного газа.
Что вам нужно
- Периодическая таблица элементов